Endergonik dan eksergonik
proses melepaskan Energi , orang yang "menghasilkan" energi, ini disebut reaksi eksergonik. Reaksi yang membutuhkan energi untuk memulai reaksi ini dikenal sebagai reaksi endergonik. Semua proses alami cenderung untuk melanjutkan sedemikian arah bahwa gangguan atau keacakan alam semesta meningkatkan (hukum kedua termodinamika).
Oksidasi / Reduksi
Reaksi biokimia dalam organisme hidup pada dasarnya adalah transfer energi. Seringkali mereka terjadi bersamaan, "terkait", dalam apa yang disebut sebagai oksidasi / reduksi reaksi. Pengurangan adalah gain dari elektron. Terkadang kami juga memiliki ion H bersama untuk naik, sehingga pengurangan juga menjadi keuntungan dari Oksidasi H. adalah hilangnya elektron (atau hidrogen). Dalam oksidasi / reduksi reaksi, satu kimia teroksidasi, dan elektron yang dilewatkan (seperti kentang panas) ke kimia (dikurangi, kemudian). Reaksi digabungkan tersebut disebut sebagai reaksi redoks. Para glikolisis proses metabolisme, Siklus Kreb, dan Fosforilasi Transportasi Elektron melibatkan transfer elektron (dalam berbagai keadaan energi) dengan reaksi redoks.
Katabolisme dan anabolisme
Anabolisme adalah seri total reaksi kimia yang terlibat dalam sintesis senyawa organik. Autotrof harus mampu memproduksi (mensintesis) semua senyawa organik yang mereka butuhkan. Heterotrof dapat memperoleh beberapa senyawa dalam makanan mereka (bersama dengan energi mereka). Bagi manusia misalnya dapat mensintesis 12 dari 20 asam amino, kita harus mendapatkan 8 lainnya dalam makanan kita. Katabolisme adalah serangkaian reaksi kimia molekul kerusakan yang lebih besar. Energi dilepaskan dengan cara ini, beberapa dapat digunakan untuk anabolisme. Produk dari katabolisme dapat dipasang kembali oleh proses anabolik menjadi molekul anabolik baru.
Enzim: Katalis Organik
Enzim memungkinkan reaksi kimia terjadi dalam batasan homeostasis dari sistem hidup. Enzim berfungsi sebagai katalis organik. Katalis adalah suatu bahan kimia yang terlibat dalam, tetapi tidak diubah oleh, reaksi kimia. Banyak enzim berfungsi dengan menurunkan energi aktivasi reaksi. Dengan membawa reaktan lebih dekat bersama, ikatan kimia dapat melemah dan reaksi akan berjalan lebih cepat dibandingkan tanpa katalis.
Enzim dapat bertindak cepat, seperti dalam kasus karbonat anhidrase (enzim biasanya berakhir dalam akhiran ase), yang menyebabkan bahan kimia bereaksi 107 kali lebih cepat dibandingkan tanpa kehadiran enzim. Karbonat anhidrase mempercepat transfer karbon dioksida dari sel ke darah. Ada lebih dari 2000 enzim yang dikenal, masing-masing yang terlibat dengan satu reaksi kimia yang spesifik. Enzim adalah substrat tertentu. Para peptidase enzim (yang memecah ikatan peptida dalam protein) tidak akan bekerja pada pati (yang diuraikan oleh manusia diproduksi amilase di mulut).
Enzim adalah protein. Fungsi dari enzim ditentukan oleh bentuk protein. Susunan molekul pada enzim menghasilkan daerah yang dikenal sebagai situs aktif di mana substrat spesifik (s) akan "cocok". Ia mengakui, batas-batas dan mengarahkan substrat dalam arah tertentu.
Hipotesis yang diinduksi menunjukkan bahwa pengikatan substrat untuk enzim pengubah struktur enzim, menempatkan ketegangan beberapa pada substrat dan selanjutnya memfasilitasi reaksi. Kofaktor adalah nonproteins penting untuk aktivitas enzim. Ion seperti K + dan Ca +2 adalah kofaktor. Koenzim adalah molekul organik nonprotein terikat enzim dekat lokasi aktif. NAD (nikotinamida adenin dinukleotida).
Jalur enzimatik terbentuk sebagai hasil dari kejadian yang biasa terjadi dari serangkaian reaksi kimia tergantung. Dalam satu contoh, produk akhir tergantung pada berhasil menyelesaikan lima reaksi, masing-masing dimediasi oleh enzim tertentu. Enzim dalam seri dapat terletak berdekatan satu sama lain (dalam organel atau dalam membran organel), sehingga mempercepat proses reaksi. Juga, produk antara cenderung tidak menumpuk, membuat proses lebih efisien. Dengan menghapus intermediet (dan oleh produk inferensi akhir) dari kesetimbangan, jalur reaktif (kecenderungan reaksi untuk membalikkan ketika konsentrasi produk membangun hingga tingkat tertentu) efek diminimalkan, karena keseimbangan tidak tercapai, sehingga reaksi akan melanjutkan ke arah yang "disukai".
Suhu: Kenaikan suhu akan mempercepat laju reaksi dimediasi nonenzyme, dan kecepatan kenaikan suhu sampai reaksi dimediasi enzim, tetapi hanya untuk satu titik. Bila dipanaskan terlalu banyak, enzim (karena mereka adalah protein tergantung pada bentuk) menjadi didenaturasi. Ketika suhu turun, enzim mendapatkan kembali bentuknya. Enzim termolabil, seperti mereka yang bertanggung jawab untuk distribusi warna pada kucing Siam dan kamuflase warna rubah Arktik, bekerja lebih baik (atau bekerja sama sekali) pada suhu yang lebih rendah.
Konsentrasi substrat dan produk juga mengendalikan laju reaksi, menyediakan mekanisme biofeedback.
Aktivasi, seperti dalam kasus chymotrypsin, melindungi sel dari bahaya atau kerusakan enzim dapat menyebabkan.
Perubahan pH juga akan mengubah sifat sesuatu benda enzim dengan mengubah bentuk enzim. Enzim juga diadaptasi untuk beroperasi pada pH tertentu atau kisaran pH.
Interaksi alosterik dapat memungkinkan enzim untuk sementara tidak aktif. Mengikat dari perubahan efektor alosterik bentuk enzim, menonaktifkan sementara itu efektor masih terikat. Mekanisme tersebut umumnya digunakan dalam inhibisi umpan balik. Seringkali salah satu produk, baik sebagai akhir atau dekat-end produk tindakan sebagai efektor alosterik, menghalangi atau shunting jalur tersebut.
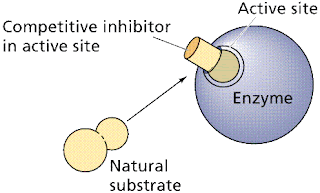
Penghambatan kompetitif bekerja dengan kompetisi dari senyawa peraturan dan substrat untuk situs mengikat. Jika cukup molekul senyawa peraturan mengikat cukup enzim , jalur dimatikan atau setidaknya melambat. PABA, zat kimia penting untuk bakteri yang menginfeksi hewan, menyerupai obat, sulfanilamide,
Penghambatan nonkompetitif terjadi ketika kimia hambat, yang tidak memiliki menyerupai substrat, mengikat enzim selain di situs aktif. Timbal mengikat kelompok SH dalam mode ini. Penghambatan ireversibel terjadi ketika bahan kimia baik secara permanen mengikat atau besar-besaran mendenaturasi enzim sehingga struktur tersier tidak dapat dikembalikan. Gas saraf secara permanen memblok jalur yang terlibat dalam transmisi pesan saraf, berakibat pada kematian. Penisilin, yang pertama dari "obat ajaib" antibiotik, permanen blok jalur bakteri tertentu digunakan untuk merakit komponen sel mereka di dinding.
Minggu, 08 April 2012
Langganan:
Posting Komentar (Atom)





















bear grylls messer
BalasHapusMy website :: bear grylls messer
bear grylls messer
BalasHapusMy page: bear grylls messer
bear grylls messer
BalasHapusmy web page - bear grylls messer
bear grylls messer
BalasHapusHere is my web-site :: bear grylls messer